
Nouvelles méthodes de marquage et de recherche d’origines natales
SCIMABIO Interface continue ses recherches pour mettre au point de nouvelles méthodes de marquage et la détection de nouveaux marqueurs naturels. Ainsi nous contribuons à lever certains verrous techniques ou méthodologiques permettant de marquer et ainsi de suivre de nouveaux stades ou de nouvelles espèces.
LPA « Inn-EAU-vaTOOLS » : vers de nouveaux outils moléculaires
L’INRAE de Thonon les Bains et SCIMABIO Interface ont décidé de mutualiser leurs compétences scientifiques et de créer le Laboratoire Partenarial Associé « Inn-Eau-vaTOOLS ». Ce laboratoire commun est dédié au développement d’outils innovants, en particulier à partir d’approches moléculaires, permettant d’améliorer les diagnoses de fonctionnalité écologique des lacs et rivières.
Mouvement et sédentarité des poissons
Nous menons plusieurs projets scientifiques destinés à mieux décrire et comprendre la diversité des mouvements observée chez diverses espèces et/ou stades de développement. Les comportements des poissons reflètent un continuum de déplacement allant de la sédentarité à la migration amphibiotique en passant par différents stades de dispersion et mobilité.
LPA « MODMAF : MOvements and Demography for the MAnagement of Fish» : Modèles démo-génétiques et statistiques d’aide à la gestion
Fruit de plusieurs années de collaboration, l’INRAE de St-Pée sur Nivelle et SCIMABIO Interface ont créé un laboratoire commun destiné à apporter un nouveau service aux gestionnaires des populations piscicoles et autres acteurs de la gestion pour faciliter l’utilisation des différents modèles (démo-génétique, statistique) comme outils d’aide à la gestion des populations piscicoles.
Répartition spatio-temporelle des habitats thermiques et refuges thermiques
SCIMABIO Interface est à l’initiative d’un consortium scientifique, regroupant le laboratoire EVS de Lyon (H. Piégay), l’Université Rennes 2 (B. Marteau), l’Université de Nottingham (S. Dugdale) et l’INRS Québec (Prof. N. Bergeron), qui collabore sur l’utilisation opérationnelle des technologies de télédétection (infra-rouge aéroporté notamment) permettant de cartographier et caractériser les habitats thermiques et refuges thermiques en rivières.
Projets
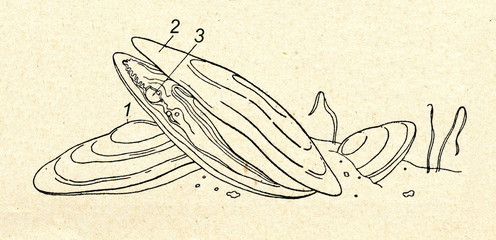
Détection de la moule perlière d’eau douce (Margaritifera margaritifera) à partir de l’ADN environnemental (ADNe)

Projet « eCray’ON »
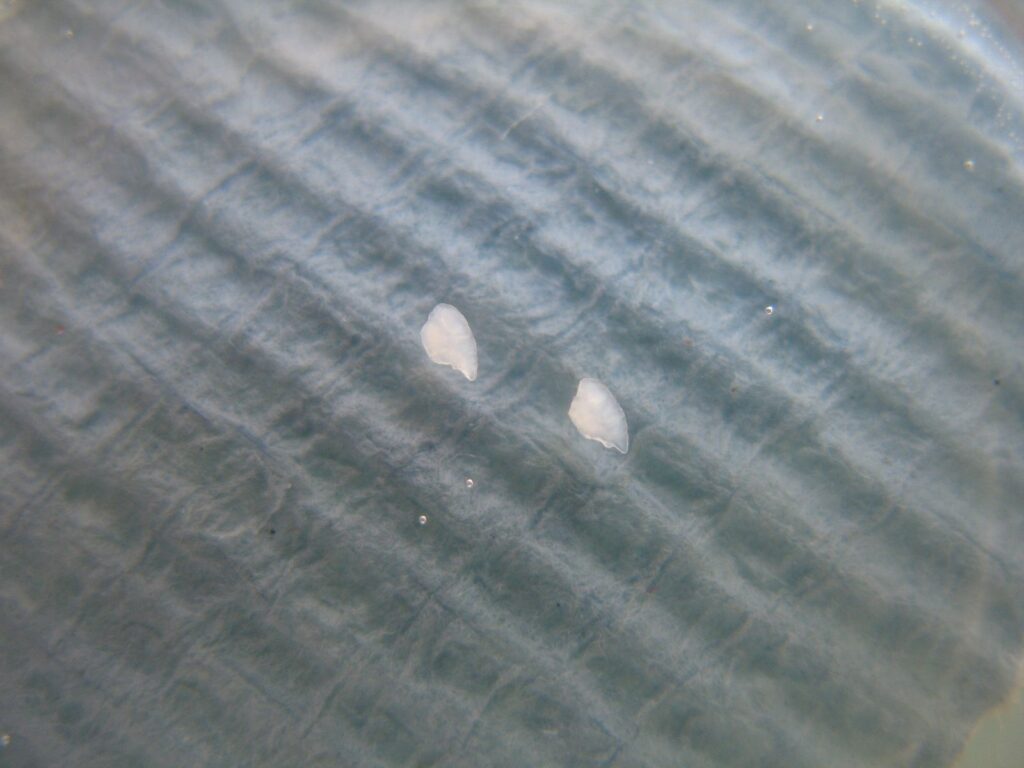
Origine natale des truites du lac du Bourget (73, Savoie)
Publications
Valentin Vasselon, Sinziana F. Rivera, Éva Ács, Salomé Baja Almeida, Karl B. Andree, Laure Apothéloz-Perret-Gentil, Bonnie Bailet, Ana Baričević, Kevin K. Beentjes, Juliane Bettig, Agnès Bouchez, Camilla Capelli, Cécile Chardon, Mónika Duleba, Tina Elersek, Clémence Genthon, Maša Jablonska, Louis Jacas, Maria Kahlert, Martyn G. Kelly, Jan-Niklas Macher, Federica Mauri, Marina Moletta-Denat, Andreia Mortágua, Jan Pawlowski, Javier Pérez-Burillo, Martin Pfannkuchen, Erik Pilgrim, Panayiota Pissaridou, Frédéric Rimet, Karmen Stanic, Kálmán Tapolczai, Susanna Theroux, Rosa Trobajo, Berry Van der Hoorn, Marlen I. Vasquez, Marie Vidal, David Wanless, Jonathan Warren, Jonas Zimmermann, Benoît Paix, 2025. Proficiency testing and cross-laboratory method comparison to support standardisation of diatom DNA metabarcoding for freshwater biomonitoring. Metabarcoding and Metagenomics, doi.org/10.3897/mbmg.9.133264
Folio D., Caudron A., Vigier L., Oddou-Muratori S., Labonne J., 2024. Using eco-evolutionary models to improve management of introgression in brown trout. Ecology of Freshwater Fish, doi.org/10.1111/eff.12789.
Bourinet F, Anneville O, Drouineau H, Goulon C, Guillard J et Richard A, 2023. Synchrony in whitefish stock dynamics: disentangling the effects of local drivers and climate. J. Limnol, 82 : 2134.
Folio D, Gil J, Caudron A et Labonne J, 2021. Genotype-by-environment interactions drive the maintenance of genetic variation in a Salmo trutta L. hybrid zone. Evolutionary Applications, 14 : 2698–2711.
Daigle A, Caudron A, Vigier L et Pella H, 2017. Optimization methodology for a river temperature monitoring network for the characterization of fish thermal habitat. Hydrological Sciences Journal, 62:3, 483-497, DOI:10.1080/02626667.2016.1242869
Gil J, Caudron A et Labonne J, 2015. Can female preference drive intraspecific diversity dynamics in brown trout (Salmo trutta, L.)? Ecology of Freshwater Fish, doi: 10.1111/eff.12215.
Richard A, O’Rourke J et Rubin J-F, 2014. External fluorescence retention of calcein-marked juvenile brown trout Salmo trutta raised in natural and artificial environments. Journal of Fish Biology, 84 : 73-84.
Richard A, O’Rourke J, Caudron A et Cattanéo F, 2013. Effects of passive integrated transponder tagging methods on survival, tag retention and growth of age-0 brown trout. Fisferies Research, 145 : 37-42.
Caudron A et Champigneulle A, 2009. Multiple marking of otoliths of brown trout, Salmo trutta L., with alizarin redS to compare efficiency of stocking of three early life stages. Fisheries Management and Ecology, 16, 219–224.
Caudron A et Champigneulle A, 2006. Technique de fluoromarquage en masse à grande échelle des otolithes d’alevins vésiculés de truite commune (Salmo trutta L.) à l’aide de l’alizarine red S. Cybium, 30(1): 65-72.


